Bạn đang xem bài viết Khí argon là gì, những tính chất, ứng dụng của khí argon tại Khoangsanvina.com bạn có thể truy cập nhanh thông tin cần thiết tại phần mục lục bài viết phía dưới.
Trên trái đất, khí argon được liệt vào danh sách các loại khí hiếm. Nó có nhiều ứng dụng trong đời sống, lĩnh vực công nghiệp của chúng ta. Để hiểu rõ hơn về khí argon, hãy cùng đọc bài viết này của Vietchem để có được những thông tin cần thiết nhé.
1. Khí argon là gì?
Khí argon – khí ar là một nguyên tố hoá học dạng khí. Nó có thể nhận diện qua những đặc điểm hoá học sau:
- Ký hiệu: Ar
- Số nguyên tử khối: 18
- Đặc điểm: Chất khí hiếm gặp
- Nhóm: 8p
- Màu sắc: Không màu
- Khối lượng mol: 39,948

Ảnh 1: Nguyên tố Ar trong bảng tuần hoàn
Các nghiên cứu khoa học chỉ ra rằng, Argon chiếm tỷ lệ khoảng 0,934% trong khí quyển. Chính vì vậy, nó là khí hiếm phổ biến nhất trên trái đất ở thời điểm này.
2. Khí argon có độc không?
Khí Argon không độc hại, không gây cháy nổ. Tuy nhiên, ở nồng độ cao hoặc trong không khí kém thông thoáng, nó có thể gây ngạt nếu làm giảm lượng oxy, dẫn đến hiện tượng thiếu oxy và gây khó thở cho con người.
3. Tính chất lý hóa của khí Argon
3.1. Tính chất vật lý
Argon thông thường tồn tại ở dạng khí, không có màu hay mùi vị, không gây độc. Loại khí này có khối lượng riêng nặng gấp 1,5 lần so với không khí. Argon có khả năng hòa tan mạnh trong nước, xấp xỉ với độ hoà tan của oxi.
Ngoài ra, khí argon còn có một số tính chất vật lý như sau:
- Nhiệt độ nóng chảy: 83,80 K /−189,35 °C/ −308,83 °F
- Nhiệt độ sôi: 87,30 K /−185,85 °C/ – 302,53 °F
- Mật sộ: 1,784 g/L
- Nhiệt lượng nóng chảy: 1,18 kJ·mol−1
3.2. Tính chất hoá học
Xét về tính hoá học, khí argon là một khí trơ. Chính vì vậy nó không phản ứng với các chất hoá học thông thường. Argon cũng không có khả năng hòa tan kim loại dù ở thể lỏng hay rắn.
3.3. Các hợp chất của khí argon là gì?
Đến tận ngày nay, chúng ta biết rất ít về các hợp chất của argon. Khi argon hoà tan vào nước có thể tạo ra các mắt lưới vì nguyên tử của nó bị mắc kẹt trong các phân tử nước.
Ngoài ra, các nhà khoa học của trường ĐH Helsinki đã thông báo về một hợp chất không ổn định tạo nên giữa argon với flo và hidro. Tuy nhiên, dù thông báo đã được phát đi từ năm 2000 nhưng nó vẫn chưa được chứng thực.
Theo thông báo đó, các nhà khoa học của Helsinki đã chiếu tia cực tím vào argon rắn chứa một lượng nhỏ HF (tức fluoride hydro). Và chất tạo được là HArF – Argon fluorohydride.
3.4. Các đồng vị của khí argon
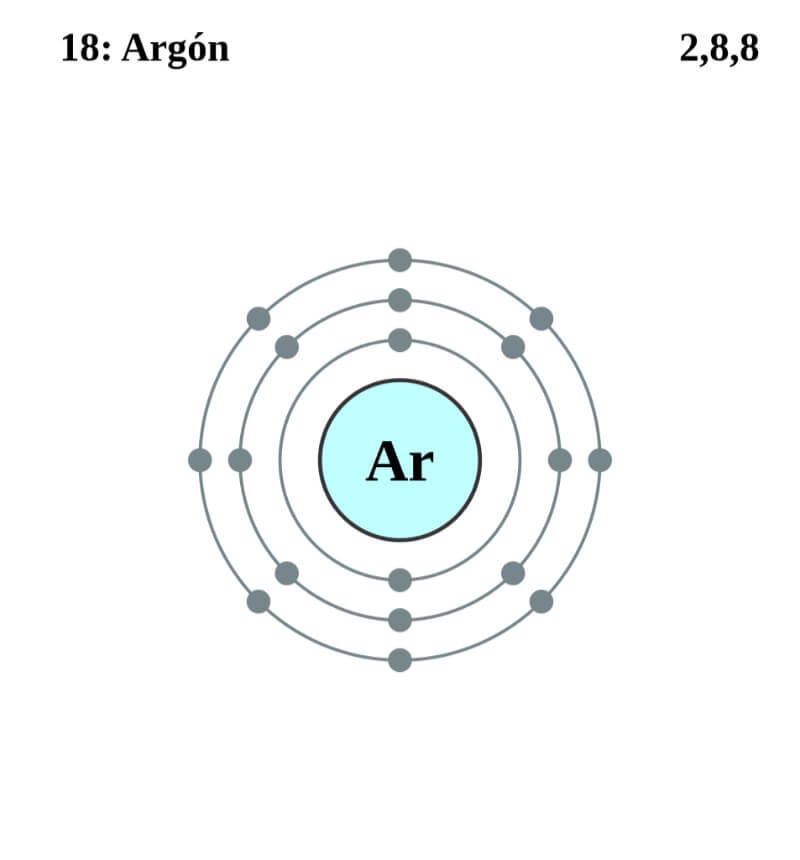
Ảnh 2: Trong tự nhiên tìm thấy argon với nhiều đồng vị khác nhau
Các đồng vị đã được xác thực là tìm thấy trên trái đất của argon là Ar40, Ar36 và Ar38. Các tính chất, đặc điểm của những đồng vị argon này đã được áp dụng trong việc tính toán niên đại của các loại đá. Điều này giúp ích rất nhiều cho các ngành khoa học, nghiên cứu khảo cổ học.
4. Khí Argon được tạo ra bằng những cách nào?
4.1. Trong tự nhiên
Trong khí quyển trái đất, khí argon được tạo ra nhờ hoạt động thông thường của các tia vũ trụ. Ở các môi trường bên dưới bề mặt trái đất, nó được tạo ra thông qua việc bắt neutron của K39 hay sự phân rã của calci, alpha…
Agon37 được tạo ra thông qua quá trình phân rã của Ca40 như là một kết quả tất yếu trong những vụ thử nghiệm hạt nhân ngầm trong lòng đất. Nguyên tố này có chu kỳ bán rã là 35 ngày.
4.2. Điều chế Argon trong phòng thí nghiệm
Hiện tại, khí argon thường được điều chế bởi các nhà khoa học. Chủ yếu, người ta áp dụng phương pháp ngưng tụ không khí ở điều kiện nhiệt độ thấp. Sau đó, tách argon khỏi oxi và nitơ để có được argon riêng rẽ.
Ngoài ra, argon cũng có thể được điều chế từ các sản phẩm thu được trong nhà máy luyện kim đen, khí thải trong quá trình sản xuất khí NH3. Argon do con người điều chế sẽ được phân chia thành 2 loại như sau:
- Khí argon thông thường với tỷ lệ argon đạt từ 99,99% trở lên;
- Khí argon có độ sạch cao với tỷ lệ argon đạt từ 99,999% trở lên;
4.3. Bảo quản và cách vận chuyển khí argon tiêu chuẩn

Ảnh 3: Bình bảo quản argon
Để bảo quản, người ta giữ khí ar trong bình thép hoặc các xitec của ô tô khi vận chuyển. Điều kiện bảo quản là giữ dưới áp suất 15 MPa hoặc 20MPa, mức nhiệt độ là 20 độ C là được.
5. Ứng dụng của khí Ar là gì?
5.1. Trong ngành luyện kim
Argon có đặc tính là khi thổi vào kim loại đang nóng chảy giúp làm giảm hàm lượng cacbon, crom. Chính vì vậy khí Ar thường được dùng làm khí thổi trong sản xuất thép, zirconium.
Khí Ar cũng được dùng để loại bỏ những hạt nhôm bên trong nhôm nóng chảy. Hay dùng làm lá chắn trong quá trình đúc một cách hiệu quả nhất.
5.2. Ứng dụng của khí argon trong lĩnh vực y học
Loại khí trơ này có công dụng lớn trong phẫu thuật lạnh. Nó giúp tiêu diệt những vùng nhỏ của các mô bệnh, cần phá huỷ. Chính vì vậy, sự có mặt của argon giúp quá trình phẫu thuật diễn ra chính xác, mang lại hiệu quả cao hơn.
Thời gian gần đây, nhiều bệnh viện và trường đại học lớn cũng sử dụng khí argon trong việc điều trị rối loạn nhịp tim. Nguyên nhân là nó có thể tấn công, tiêu diệt các tế bào cản trở xung điện thông thường.
5.3. Ứng dụng của khí argon trong cuộc sống
- Sử dụng trong sản xuất bóng đèn sợi đốt dùng hàng ngày
- Độn giữa các tấm kính của khung cửa sổ cách nhiệt
- Bảo quản rượu một cách hiệu quả nhờ ar sẽ giúp rượu không bị lên men quá mức hay biến chất

Ảnh 4: Argon có nhiều ứng dụng quan trọng trong cuộc sống
Như vậy, bạn đã có đầy đủ thông tin cần thiết về khí argon cũng như những ứng dụng của nó. Hy vọng những thông tin này giúp bạn hiểu hơn về khí hiếm argon cũng như ảnh hưởng của khí ar trong đời sống nhé.
Cảm ơn bạn đã xem bài viết Khí argon là gì, những tính chất, ứng dụng của khí argon tại Khoangsanvina.com bạn có thể bình luận, xem thêm các bài viết liên quan ở phía dưới và mong rằng sẽ giúp ích cho bạn những thông tin thú vị.
